2024年11月,FDA正式发布了《非脊柱骨板、螺钉和垫圈的510(k)提交建议》指南。本文将从以下几个方面解读该指南的核心内容,为企业合规操作提供实用建议。

一、指南的适用范围
该指南仅适用于II类骨科非吸收性非脊柱骨板和螺钉系统、独立骨螺钉以及相关的垫圈,不包含以下设备:用于脊柱、下颌骨、颅面骨及眼眶骨折修复的设备,以及可吸收或表面经过涂层处理的设备等。具体适用的Product Code如下:
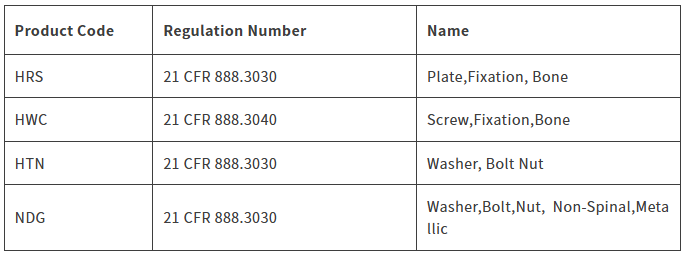
二、指南的核心内容
1. 510(k)提交的建议
指南为企业提供了一系列关键的510(k)提交建议:
使用说明:要求明确设备的解剖学应用部位(如股骨、胫骨)及其用途(如骨折固定、关节融合)。
设备描述:需详细列出设备的关键参数,包括材料组成、尺寸范围及兼容的螺钉或配件等,并建议以表格形式呈现设备规格。
对比分析:制造商应通过对比具备法律营销许可的等效设备,证明其产品的实质等效性。
2. 测试和合规要求
针对性能验证,指南提出了一系列详细要求:
机械性能测试:包括板材的弯曲测试、螺钉的抗扭强度、拔出强度测试等,需基于ASTM标准进行,并建议采用表格展示测试数据与对比结果。
生物相容性:要求所有与患者接触的材料符合ISO 10993-1标准,确保对人体无害。
磁共振兼容性:设备需评估在磁共振环境中的安全性和兼容性,如设备的位移风险、发热情况及成像伪影。
3. 其他关注点
灭菌与包装:提供灭菌设备的包装说明和保质期测试方法,确保无菌状态和包装完整性。
修改与豁免:企业如需对既有设备进行改进,需提交详细的性能测试结果和工程分析。
4. 指南的附录A提供了骨板性能测试的推荐方法和数据总结的示例,附录B针对骨螺钉的机械性能测试提供了详细说明,供企业参考使用。
三、总结
该指南为非脊柱骨板、螺钉和垫圈设备的制造商提供了清晰的合规方向和技术要求。企业在产品设计与监管提交中,应充分利用指南提供的框架,确保设备的安全性和有效性。





 沪公网安备 310114020088*8号
沪公网安备 310114020088*8号