企业在申请FDA 510k 或者场地注册/产品列名之前,需要在FDA有个付费账号用于付款。对于非美国企业,申请该付费账号需要邓白氏编码。(注:若早期已在美国列名过医疗器械产品,则应该已经申请过邓白氏编码)
邓白氏编码的申请步骤
1、点击:链接 进入官方网站
2、点击下图红框的“立即申请”
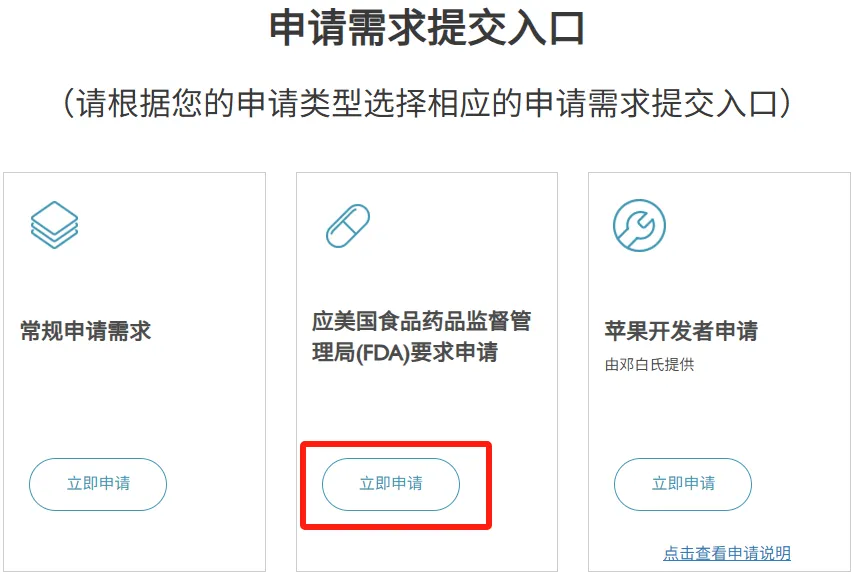
3、用户注册
使用手机号进行免费注册,成功注册后使用账号密码登入
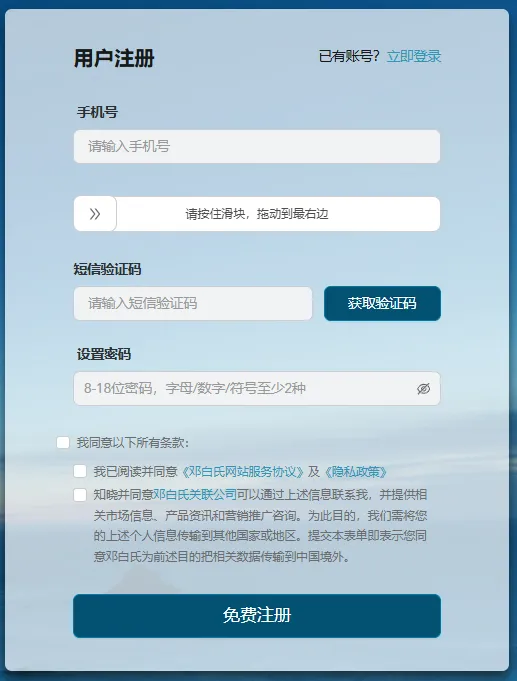
4、企业认证审核(企业核验)
申请“邓白氏编码”需先完成企业核验。
如下图所示:成功登入后将会进入如下图所示的页面,点击图中右下角的“下一步”
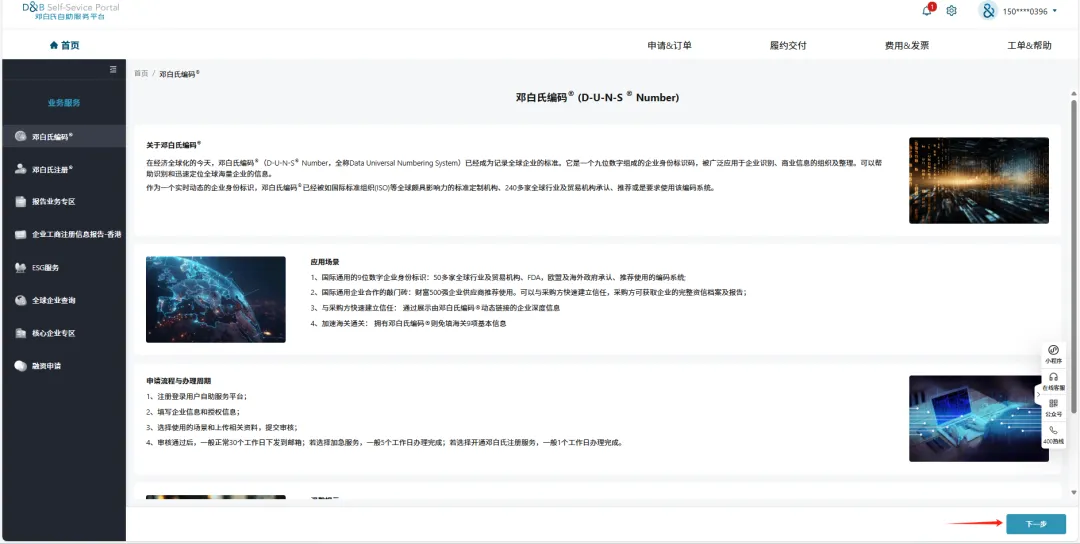
如下图所示:页面跳转提示“前往认证”
页面将跳转显示“实名核验”相关要求,点击:“我知道了”
页面跳转如下图所示,按要求填写“企业信息”、“授权信息”以及“法定代表人信息”后提交申请
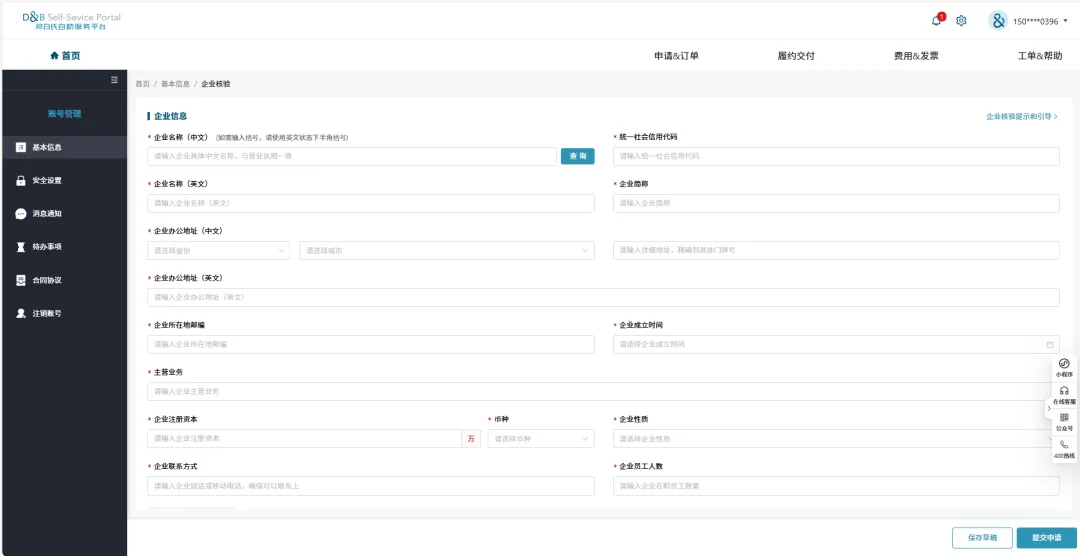

5、免费申请邓白氏编码——填写申请信息
添加核验成功的企业,选择使用的场景(美国食药监局(FDA)上传相关资料,提交审核;
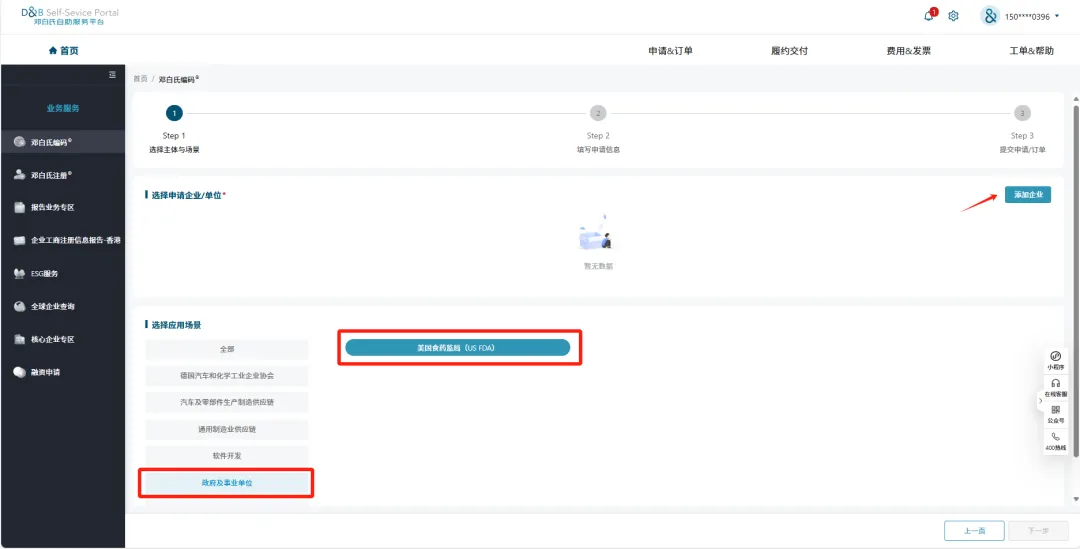
将FDA提供的邮件截图证明,发给平台进行审核,正常免费申请 30天会拿到邓白氏编码。
注:若有其它需求,平台也提供定制化收费服务。具体费用平台会根据不同的服用进行定制化收费。
FDA 付费账号(User Fee System)申请步骤
1、点击:链接 进入FDA官方网站
2、点击“New User? Please register...”
3、选择“I am a new FDA User Fee Organization”并点击 “Go”
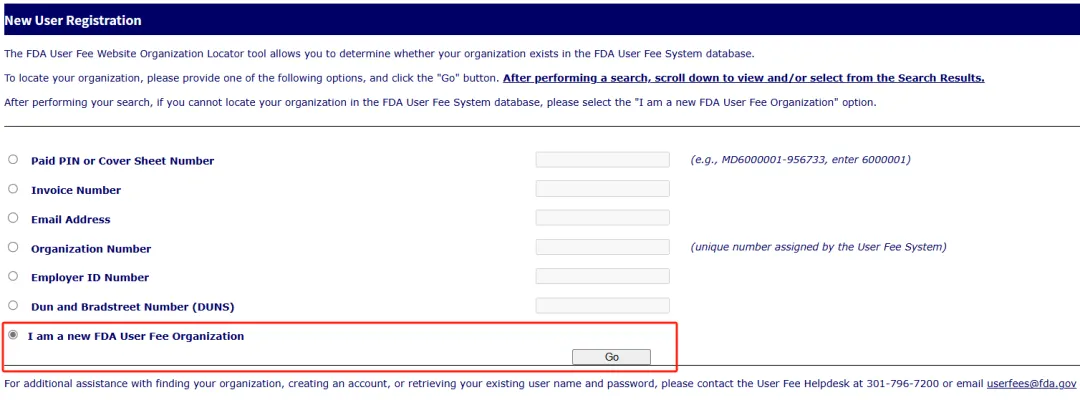
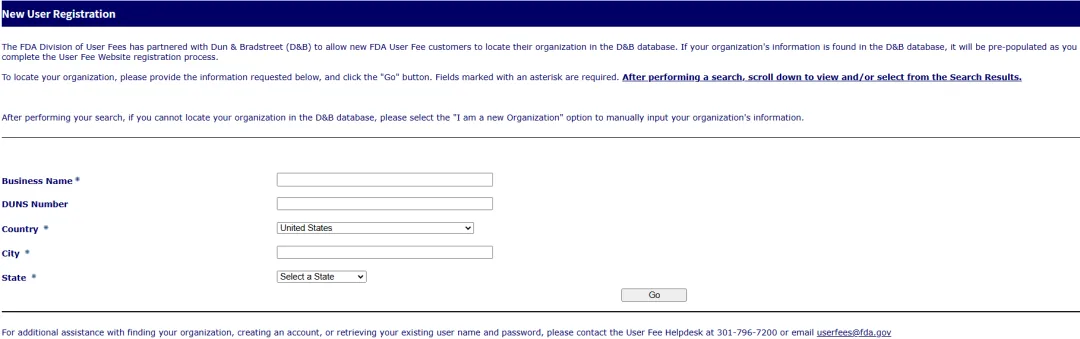
4、填写信息
按要求填写信息,此时如果拿到邓白氏编码,填写页面会跳出关联的公司名。点击确认后会跳转到另一个信息填写界面,其中包括联系人信息,公司信息,密码等。全部填写完成就可以生成账号了。
小企业申请FDA CDRH的优惠政策
年销售额低于1亿美金的企业可以申请小企业资质,享受优惠的产品注册费用。
有资格获得小企业费用减免的申请类型包括:Premarket Notification (510(k)), De Novo request, Premarket Applications (Premarket Approval Application [PMA], Biologics License Application [BLA], Product Development Protocol [PDP]), Premarket Report (PMR), PMA/BLA Supplements and PMA Annual Reports, 30-day-notices, and 513(g) request for classification information.
申请小企业资质的步骤
点击:链接 查看小企业申请指南
收集税务文件(最近的财政年度,一个财政年度指的是从10月1日到次年的9月30日)。
获取 Organization ID number (Org ID).——该ID在申请完FDA付费账号后可查询到。
在FDA官网下载最新的小企业申请表《FDA Form 3602A》。
填写 FDA 小型企业认证申请表格 FDA Form 3602A (需要使用Adobe Acrobat PDF,WPS不兼容),并获得税务局盖章。
将所有文件(税务文件和 FDA 表格)发送至以下地址:
FY 20__ MDUFA Small Business Qualification
Small Business Certification Program
10903 New Hampshire Avenue
Building 66, Room 5305
Silver Spring, MD 20993
U.S.A.
FDA将在收到小企业认证申请后的60天内完成对小企业认证申请的审核。
注:关于该政策的详细信息可在点击:链接 进入官方网站的相关页面进行查询。





 沪公网安备 310114020088*8号
沪公网安备 310114020088*8号